
| 販売名 | Alofisel® |
| 一般的名称 | darvadstrocel |
| 製造販売者 | Takeda Pharma A/S |
| 対象疾患 | 非活性/軽度活性管腔クローン病成人患者の 肛門周囲複雑瘻孔 (complex perianal fistulas in adult patients with non-active/mildly active luminal Crohn’s disease) |
| 承認日 | 2018年3月23日 |
| 薬価 | £54,000.00/4 vials (≒826万2000円) 1£=153円 |
| 関連文書 | 添付文書 (SmPC) 患者説明資料 (Package leaflet: Information for the patient) |
【製品概要】
Takeda Pharmaceutical社 Alofiselサイト
Alofiselは非活性/軽度活性管腔クローン病成人患者における肛門周囲複雑瘻孔(complex perianal fistulas in adult patients with non-active/mildly active luminal Crohn’s disease)を対象とする他家脂肪由来幹細胞製品です。ベルギーのTiGenix社が開発し、2016年に米国以外の権利を武田薬品にライセンスアウトしています(その後、2018年にTiGenix社は武田薬品に買収)。
英国における1治療(4バイアル)あたりの薬価は5万4000ポンド(≒826万2000円)となっています。
2018年3月にEUでの承認を取得しました。日本では2021年2月に製造販売承認申請が行われており、また、米国では第III相治験が進行中です。
【対象疾患】
クローン病成人患者の肛門周囲複雑瘻孔
クローン病は小腸や大腸などの消化管に炎症が起きる慢性炎症性腸疾患で、日本国内の患者数は約7万人です。また海外では欧米での発症率が高く、罹患率は1000人当たり3.2人となっています。肛門周囲複雑瘻孔はクローン病の合併症の1つです。潰瘍が腸壁を完全に貫通した状態が瘻孔(ろうこう)であり、瘻孔が進み肛門の周辺に孔が形成された状態が肛門周囲複雑瘻孔です。
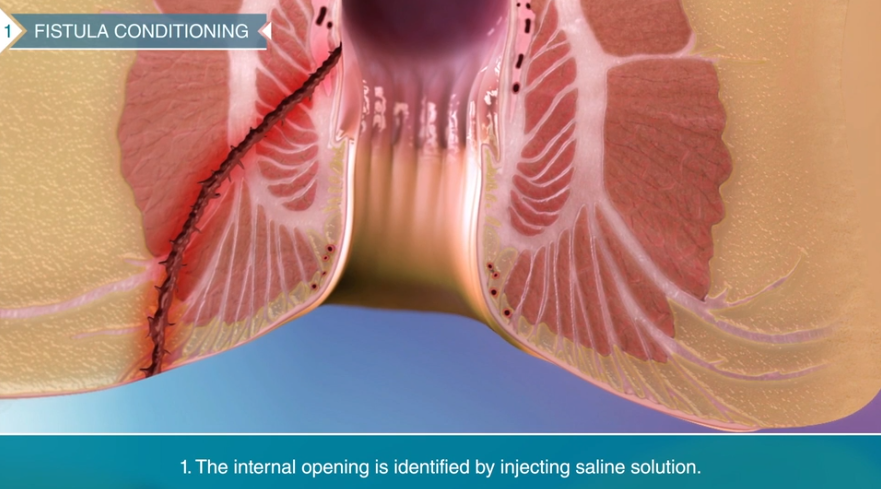
【作用メカニズム】
Alofiselによる 治療では、瘻孔の周辺部に1.2×106個(120万個)の細胞が注射投与されます。
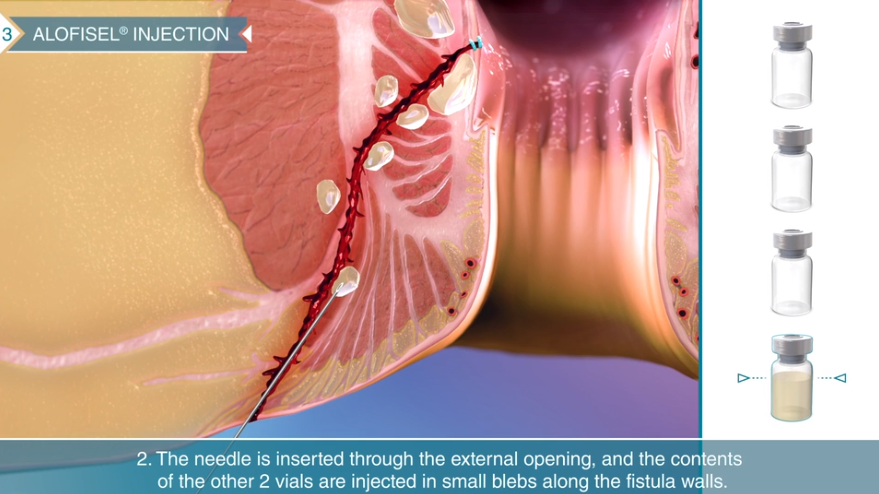
瘻孔では細菌感染症や糞便汚染により局所炎症が起こり、さらに炎症部位では活性化されたリンパ球の浸潤とIFNγ等の炎症性サイトカインの局所放出が起こります。脂肪幹細胞であるAlofiselは、これらの活性化リンパ球の増殖を阻害し、炎症性サイトカインの放出を減少させることで炎症を抑制し、瘻孔周辺の組織を回復させると考えられています。
【製品特徴】

Alofiselは細胞懸濁液をバイアルに充填した形状で、同じく間葉系幹細胞製品であるテムセルやステミラックが凍結保管であるのに対して、Alofiselは室温(15-25℃)で保管されます。そのため有効期間が48時間と短く、他家細胞製品ではありますが治療が決まってからのオーダーメイドとなります。製造所において脂肪から取り出された細胞は中間製品の段階で凍結保管されており、オーダー後に最終培養を行い1週間ほどで医療機関に届けられます。凍結保管品に比べて有効期間が短い一方で、医療機関での取り扱いが容易であるという利点があります。
