
| 販売名 | ハートシート® |
| 一般的名称 | ヒト(自己)骨格筋由来細胞シート |
| 製造販売者 | テルモ株式会社 |
| 対象疾患 | 虚血性心疾患による重症心不全 |
| 承認日/保険収載日 | 2015年9月18日(条件及び期限付承認) /2015年11月26日 |
| 保険償還価格 | 採取・継代培養キット:6,480,000円 回収・調製キット:1枚当たり1,710,000円 |
| 関連文書 | 添付文書 (PMDAウェブサイト) 審査報告書 (PMDAウェブサイト) 申請資料概要 (PMDAウェブサイト) |
【製品概要】
テルモ社 ハートシートサイト”再生医療で心不全に挑む”
ハートシート®は、自己の骨格筋(標準的には大腿筋)から採取・培養した骨格筋芽細胞シートです。虚血性心疾患に起因する重症心不全の治療として、心臓表面に貼付移植として使用されます。大阪大学心臓血管外科の澤芳樹 教授らが開発した心筋細胞シートを元に大阪大学とテルモ株式会社の共同研究で開発され、2015年に条件及び期限付承認制度の適用第一号として、テルモ社が再生医療等製品の製造販売承認を取得しました。保険償還はJ-Tec社のジェイスやジャックと同様に採取・継代と回収・調製に分けられています。1回の治療の5枚のシートを使用するため、1回あたりの治療費は1503万円となります。
2023年9月に正式承認申請を行ったものの、2024年7月19日の厚生労働省 薬事審議会において有効性が確認できないとして正式承認の了承を得られなかったことから、販売終了となります。
テルモ株式会社 プレスリリース「厚生労働省 薬事審議会における「ハートシート」の審議結果について」
【対象疾患と作用メカニズム】
対象疾患
虚血性心疾患、心臓弁膜症、拡張型心筋症、先天性心疾患等により心臓のポンプ機能が著しく低下し、十分な血液を全身に送り出すことができない状態が心不全であり、さらに心機能の低下が重度のものが重症心不全です。この内、虚血性心疾患に起因し、かつ薬物治療や侵襲的治療を含む標準治療で効果不十分な重症心不全がハートシート®の適応対象となります。
作用メカニズム
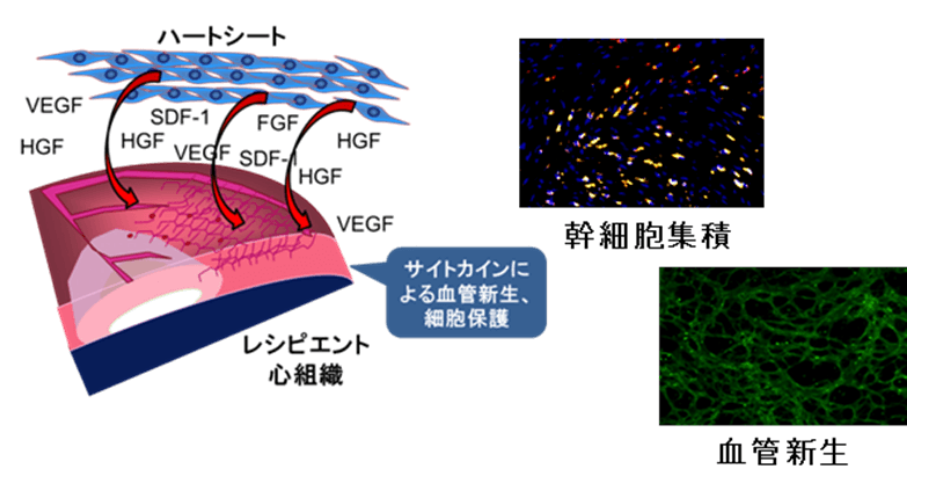
ハートシート®の作用メカニズムは、開発当初は骨格筋の収縮力による心機能の補助と考えられていましたが、後の研究により、ハートシート®から分泌されるVEGFやHGFなどによる血管新生や幹細胞の集積、細胞保護と考えられています。
【治療の流れ】
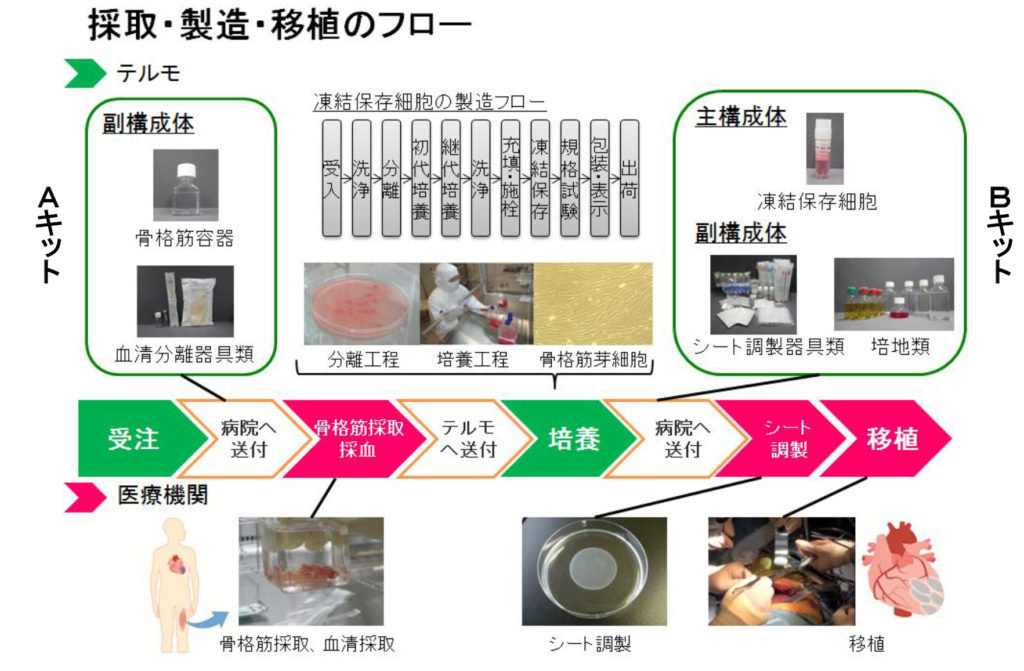
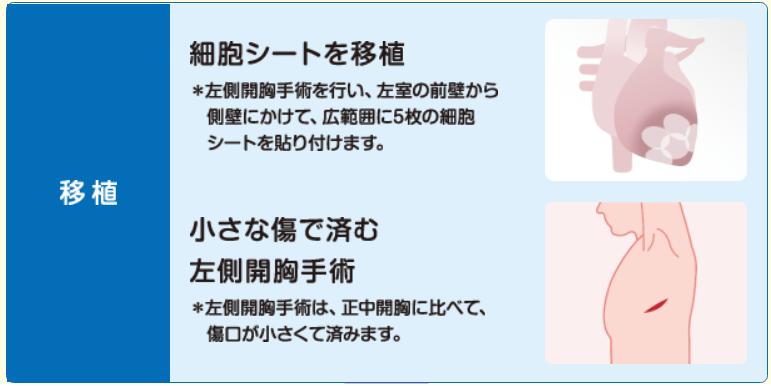
医療施設で患者の大腿部から採取された骨格筋(2-5g程度)から、テルモ社の培養施設で骨格筋芽細胞が分離され、患者自身の血清を含む培養培地中で約7週間培養されます。その後、細胞の状態で医療施設に送られ、医療施設において3日間のシート培養が行われた後に手術に用いられます。このシート培養では、セルシード社の温度応答性細胞培養器材が使われています。移植は、左側開胸手術により左室の全壁から側壁にかけて5枚のシートを貼り付けます。
【条件及び期限付承認】
ハートシート®は、条件及び期限付承認制度の第1号として承認を受けました。条件及び期限は以下の通りとなっています。
条件:
1. 緊急時に十分対応できる医療施設において、重症心不全及び開胸手術に関する十分な知識・経験を持つ医師のもとで、臨床検査による管理等の適切な対応がなされる体制下で本品を使用すること。
2. 条件及び期限付き承認後に改めて行う本品の製造販売承認申請までの期間中は、本品を使用する症例全例を対象として製造販売後承認条件評価を行うこと。
期限:
5年間で60症例のデータを収集し、120例の対照と比較すること。その後、医療機関との契約に時間を要したこと等により十分な症例が集まっていないことから、期限が3年延長されています。
正式承認審査結果:
2023年9月に正式承認申請を行いましたが、2024年7月19日の薬事審議会において、主要評価項目である心臓疾患関連死までの期間、および副次評価項目である心機能に関するLVEFの改善などについて対照群に対して優越性は示されないとして、正式承認には至りませんでした。
【Nature誌からの批判】
ハートシート®に適用された条件及び期限付早期承認制度について、Nature誌が批判的な記事を掲載しています。 ハートシート®は、7名の第II相臨床試験の結果を元に申請され、早期承認を受けました。この段階では安全性の証明と有効性の示唆であり、正式な承認ではなく、承認後5年(ハートシート®では8年間に延長)以内に一定数の臨床データを揃え、その結果をもって再度審査を受け、正式承認に至ります。この再審査は第III相臨床試験と同等に厳しく行われますが、その間の治療費は健康保険および患者の負担で行われるため、見方を変えると通常莫大な費用をかけて製薬会社が行う第III相臨床試験を、患者や国に費用を肩代わりさせて行っているともとれることになり、Nature誌はその点を批判しています。これに対して、高橋政代 理化学研究所プロジェクトリーダー(当時)は、新しいシステムはそういった危険性ははらむものの、ハートシート®は標準的な治療では効果がない重い心臓機能障害に対するもので、心臓移植のドナー不足の問題がより顕著な日本では唯一の治療法であり、それをタイムリーに提供することは患者への利益のためであり、製薬企業の利益のためではない旨の見解を日本再生医療学会雑誌中で述べています。
