
〇他家骨髄由来間葉系幹細胞を用いた、中枢神経系疾患に対する細胞医薬の開発
〇慢性期脳梗塞については、第IIb相臨床試験において主要評価項目未達(2019年1月発表)
〇慢性期外傷性脳損傷については、第II相臨床試験において主要評価項目を達成し、先駆け審査指定制度の対象品目に指定
| 会社名 | サンバイオ株式会社 SanBio Company Limited |
| 所在地 | 東京都中央区明石町8-1 聖路加タワー28F |
| 代表者 | 代表取締役社長 森敬太 代表取締役会長 川西徹 |
| 設立 | 2001年2月(米国カリフォルニア州)/ 2013年2月27日(日本) |
| 上場 | 2015年4月8日 マザーズ (4592) |
【会社概要】
他家骨髄由来間葉系幹細胞を用いて、中枢神経系疾患に対する細胞医薬の開発を行っている企業です。慢性期脳梗塞,慢性期外傷性脳損傷を始めとして複数のパイプラインの開発が進められています。
脳神経の再生医療分野で世界的に有名な慶應義塾大学の岡野栄之教授を科学アドバイザーに迎え、2001年にサンフランシスコ・ベイエリアにてSanBio, Incとして創業されました。その後、2013年に日本法人サンバイオ株式会社を設立、本社化し、2015年4月にマザーズに上場しています。
社名は、太陽(Sun)ではなく、創業地のSan Francisco bay areaの”San”に由来しているものと思われます。
【事業内容】
開発パイプライン
2019年9月現在、下記の各パイプラインの開発が進行中です。
①再生細胞医薬SB623
健常者ドナーの骨髄から抽出・培養した他家骨髄由来間葉系幹細胞です。
ドナーの骨髄から採取した間葉系幹細胞に、神経再生能力を高めるための遺伝子(Notch 1)を一過性に導入し、その細胞を大量培養して量産化するプロセスを確立しています。
②治療方法とメカニズム
脳梗塞患者に対して、頭蓋に1cm程度の穴を開け、そこから細胞を脳内に直接移植します。長期入院も不要で、臨床試験では被験者は翌日には退院しています。また、免疫抑制剤も不要です。
治療メカニズムとしては、投与されたSB623は脳内に生着して神経細胞へと変化するわけではなく(SB623は投与後1ヶ月以内には患者体内から消失します)、主に以下の作用により患者の細胞を刺激し、再生のトリガーとして働きます。
(1) 神経幹細胞を損傷部位に誘導する(バイオブリッジ)
(2) SB623が分泌するFGF-2等の成長因子や細胞外マトリックスにより、神経細胞の増殖や血管新生が誘導される。
開発状況
SB623について、慢性期脳梗塞、慢性期外傷性脳損傷に対する臨床試験が進められています。
脳梗塞については、米国での開発においては第IIb臨床試験から大日本住友製薬との共同開発となっています。日本国内での開発については、2009年に開発実施権および販売権を帝人ファーマにライセンスアウトしていましたが、上市に向けた開発のスピードアップのためサンバイオ単独で開発を行うことを理由として、2018年2月に両権利が返還されています。
①SB623/慢性期脳梗塞
脳梗塞とは、脳の動脈が詰まることで脳の神経細胞が壊死し、運動障害,感覚障害,言語障害といった深刻な後遺症が残る疾患です。患者数は日本国内で78万人、米国では574万人とされています。
脳梗塞発症後6ヶ月から90ヶ月が経過した運動機能障害がある慢性期の患者に対する臨床試験の結果、第I/IIa相臨床試験では安全性が確認され、運動機能改善の有効性が示唆されました。しかし、その後実施された第IIb相臨床試験では、安全性の問題は見られなかったものの有効性については主要評価項目未達となったことが2019年1月に発表されました。
今後は、試験結果の詳細解析後、引き続き開発を進める方針となっています。
②SB623/慢性期外傷性脳損傷
外傷性脳損傷とは、交通事故や転倒,またはスポーツ等により頭に強い衝撃が加わることで脳に損傷が起こり、半身麻痺や感覚障害,記憶障害,高次脳機能障害といった深刻な後遺症が残る疾患です。日本国内の患者数は4万人ですが、米国においては530万人であり、毎年28万人が新たに発症しているとされています。
脳損傷受傷後12ヶ月以上が経過した慢性期外傷性脳損傷患者に対する第II相臨床試験の結果、統計学的に有意な運動機能の改善を認め、主要評価項目を達成したことが2018年11月に発表されています。
この結果を基に厚生労働省に再生医療等製品として「先駆け審査指定制度」の申請を行い、2019年4月に対象品目として指定されました。また同月に欧州医薬品庁より先端医療医薬品の指定も受けています。
開発ベンチャーから製薬企業へ
同社は今後、研究開発ベンチャーから、開発,製造,販売まですべてを手掛ける製薬企業へと転換する方針を掲げています。その体制構築の一つとして、2019年8月に再生医療等製品製造販売業許可を取得しています。
また同社ウェブサイトに”世界トップレベルの開発体制”とあるように、下記に挙げる方を始め同社にはこの分野での第一人者が多く集まっています。
・創業科学者 岡野栄之 博士 (慶応義塾大学教授。脳神経領域の再生医療、iPS研究における第一人者)
・科学顧問 George R. Martin 博士 (元米国NIH老化研究所所長。ラミニンの発見者)
・科学顧問 Arnold Caplan博士 (ケースウェスタンリザーブ大学総合医学教授。間葉系幹細胞の発見者で、間葉系幹細胞分野における世界の第一人者)
・シニア・アドバイザー Donald Kennedy 博士 (元スタンフォード大学学長,元米国食品医薬品局(FDA)長官,元Science誌編集長)
・シニア・アドバイザー Damien Bates 博士(世界で初めて同種移植系生物製剤を承認)
サンバイオショック
慢性期脳梗塞の第IIa相臨床試験の結果公表後、同社の株価が約1/5に急落しました。当時の同社の時価総額がマザーズ市場全体の約10%を占めるなど非常に影響力の強い企業だったこともあり、その影響はほかのバイオ関連株や新興市場全体に及び、一部では「サンバイオショック」とも呼ばれました。
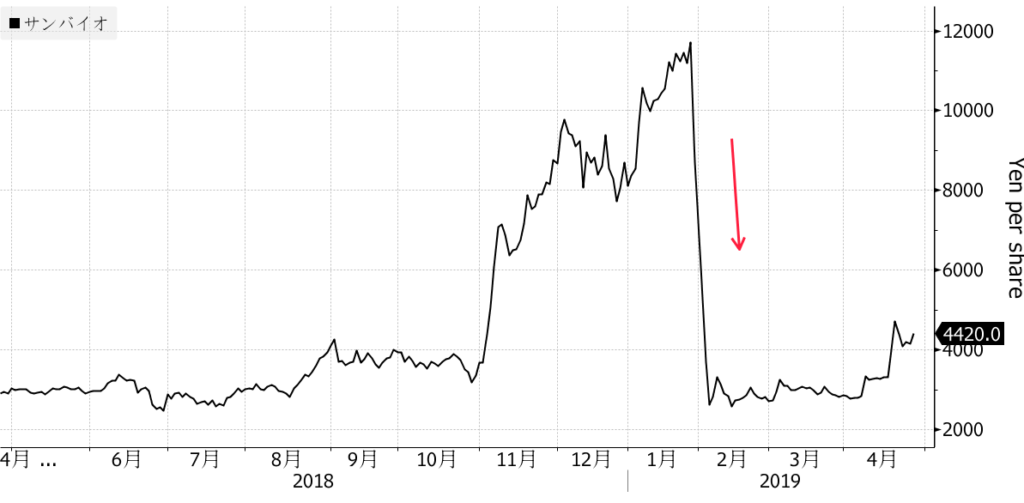
これは、それだけ脳梗塞に対する治療薬に対する期待が大きかったことを示す一方で、同社,SB623の全体像,および再生医療のことを十分に理解する前に、臨床試験の公表結果のみを見て、投機的に株を売買した個人株主が相当数いたのではないかと考えられます。
米国などと比較して、日本ではある技術分野の専門家が投資機関のアナリストになるケースが非常に少なく、そのため再生医療のような新しい分野には投資機関が参入しづらい構造となっています。その結果、先述のような投機目的の個人投資家の比率が高くなり、株価が安定しづらくなるという問題があります。
今回の同社の株価の推移も、この構造的な問題が大きく影響していると考えられます。これは同社のみでなく、バイオ関連を含めた新興テクノロジー企業全体に共通の問題となっています。
